Прогностические факторы возникновения рецидива пролапса гениталий

Филимонов В.Б., Васин Р.В., Васина И.В., Каприн А.Д., Костин А.А.
Сведения об авторах:
- Филимонов В.Б. – заведующий кафедрой урологии и нефрологии ФГБОУ ВО РязГМУ Минздрава России, Государственное бюджетное учреждение Рязанской области «Городская клиническая больница № 11», Рязань, v.filimonov@rzgmu.ru, AuthorID 695390
- Васин Р.В. – к.м.н., врач уролог, доцент кафедры урологии и нефрологии ФГБОУ ВО РязГМУ Минздрава России, заместитель главного врача по хирургической помощи и организационной работе ГБУ РО «ГКБ № 11», rw@mail.ru, AuthorID 763346
- Васина И.В. – гинеколог, Государственное бюджетное учреждение Рязанской области «Городская клиническая больница № 11», gkb11rzn@yandex.ru, AuthorID 763488,
- Каприн А.Д. – д.м.н., профессор, академик РАН, генеральный директор ФГБУ «НМИЦ радиологии» Минздрава России, заведующий кафедрой урологии и оперативной нефрологии с курсом онкоурологии медицинского факультета Медицинского института РУДН, contact@nmicr.ru, AuthorID 96775
- Костин А.А. – профессор кафедры урологии и оперативной нефрологии с курсом онкоурологии медицинского факультета Медицинского института РУДН; заведующий кафедрой урологии,
онкологии и радиологии ФПК МР Медицинского института РУДН, г. Москва, kostin@nmirc.ru, AuthorID 193454
DOI: 10.29188/2222-8543-2019-11-2-152-157
Актуальность оперативного лечения пролапса гениталий (ПГ) не вызывает сомнения, в связи со значительной распространенностью ПГ у женщин (11,4–41%) и риском операции по поводу этого заболевания (2,7–11%) [1]. Оперативное лечение ПГ остается единственным эффективным методом лечения. При этом операции по устранению ПГ с использованием современных полипропиленовых сеток, создающих надежный каркас для органов таза, являются патогенетически обоснованными, так как основываются на «замене» поврежденной и неполноценной тазовой фасции на новую (неофасциогенез) [2,3].
Несмотря на преимущества использования полипропиленовых сеток, эффективность которых достигает 81–95,8% [4-9], проблема безопасности их применения остается актуальной, так как это сопряжено с риском специфических осложнений: эрозий слизистой влагалища и мочевого пузыря, синехий влагалища, уретро-влагалищных свищей, сморщиваний протеза, хронического болевого синдрома, инфицирования и экструзии сетки [4, 6].
Одним из направлений профилактики возникновения осложнений, связанных с постановкой во влагалище сеток, является усовершенствование сетчатых имплантатов (уменьшение поверхностной плотности и площади соприкосновения с тканями без уменьшения формоустойчивости) и способов их установки [10, 11].
С целью профилактики осложнений, обусловленных применением сеток при ПГ, проведен ряд работ, посвященных разработке показаний к использованию синтетических полипропиленовых сеток [9, 12, 13, 14].
Авторы считают необходимой экстраперитонеальную кольпопексию сетчатым имплантом при ПГ только в случае повышенного риска рецидива заболевания: при тяжелых степенях дисплазии соединительной ткани (ДСТ); при наличии дефекта тазовой фасции, тяжелых (III–IV степени) и рецидивных форм ПГ, наличии экстрагенитальных заболеваний; пожилым женщинам; при ожирении. Существует необходимость в углубленном изучении факторов, влияющих на развитие рецидива ПГ, и обосновании объективных критериев отбора пациенток для оперативного лечения с использованием собственных тканей или с помощью полипропиленовых сеток. Цель исследования: разработать критерии отбора пациенток для оптимального метода оперативной коррекции ПГ влагалищным доступом с использованием собственных тканей или полипропиленовых имплантатов.
МАТЕРИАЛЫ И МЕТОДЫ
Согласно цели исследования проведено проспективное исследование, в которое были включены 93 пациентки старше 18 лет с симптомным ПГ II–IV стадии по классификации POP-Q, согласившихся на оперативное лечение и участие в данном исследовании.
Критерии исключения:
- беременность;
- облучение малого таза в анамнезе;
- тяжелые сопутствующие соматические заболевания, являющиеся абсолютным противопоказанием к оперативному лечению;
- изолированное ректоцеле;
- острые воспалительные процессы органов малого таза;
- злокачественные и предраковые заболевания гениталий;
- невозможность наблюдать пациентку в течение 24 мес после операции;
- поливалентная аллергия, в связи с риском развития реакции отторжения полипропиленового имплантата.
Рандомизация исследования проводилась методом «слепых конвертов», в результате пациентки были разделены на две группы в зависимости от способа коррекции ПГ. В 1-ю группу (n=43) вошли женщины, которым была выполнена влагалищная операция с использованием собственных тканей; во 2-ю (n=50) – пациентки, оперированные по разработанному нами способу вагинальной экстраперитонеальной кольпопексии перфорированным сверхлегким (поверхностная плотность 19 г/м2) полипропиленовым имплантатом (патент РФ №2538796, заявка на изобретение №2013102790/14 от 05.02.2013, опубл. 10.01.2015)[15]. Хирургические методы были стандартизированы. Характер выполненных операций представлен в таблице 1.
Таблица 1. Объем выполненных оперативных вмешательств, %
| Название операции | Группа | |
|---|---|---|
| I | II | |
| Коррекция переднего отдела тазового дна сеткой | 0 |
100,0* |
|
Коррекция заднего отдела тазового дна сеткой |
0 |
20,0 |
|
Пластика передней стенки влагалища собственными тканями |
100* |
0 |
|
Пластика задней стенки влагалища местными тканями |
18,6* |
0 |
|
Влагалищная гистерэктомия по Мейо с кульдопластикой по Макколлу |
23,3 |
18,0 |
|
Ампутация шейки матки по Штурмдорфу |
4,7 |
4,0 |
|
Ампутация шейки матки по Шредеру |
16,3 |
14,0 |
|
Пластика шейки матки методом расслоения по Ельцову-Стрелкову |
4,7 |
6,0 |
|
Перинеолеваторопластика |
72,1 |
66,0 |
Примечание — *различия достоверны при сравнении показателей 1 группы со II группой (р<0,05)
Пластику передней и задней стенок влагалища, перинеолеваторопластику, влагалищную гистерэктомию по Мейо с кульдопластикой по Макколлу, экстирпацию матки трансабдоминальным доступом, ампутацию шейки матки по Шредеру и Штурмдорфу, пластику шейки матки методом расслоения по ЕльцовуСтрелкову, проводили по известным методикам [16, 17].
Основные хирургические приемы предложенного способа коррекции ПГ заключаются в следующем:
- широкое выделение паравагинального пространства с обязательной мануальной идентификацией необходимых анатомических ориентиров;
- использование двух рукавов, перфорирующих обтураторные отверстия;
- подготовка импланта из легкой полипропиленовой сетки в форме равнобедренной трапеции с перфорационными отверстиями для уменьшения массы сетки и площади соприкосновения импланта с тканями;
- подготовка импланта индивидуальных размеров с целью перекрытия дефектов фасций;
- субфасциальная установка импланта и тщательное его расправление без натяжения, с фиксацией заднего края сетки к парацервикальным тканям при сохранении матки или к шву по МакКоллу при выполнении гистерэктомии, а переднего края — к лобково-шеечной фасции у переднего разреза влагалища;
- ушивании раны влагалища без иссечения слизистой.
Всем пациенткам в предоперационном периоде для установления диагноза и показаний к оперативному вмешательству, определения объема операции было проведено комплексное клиническое, лабораторное и инструментальное обследование. Клиническое обследование включало сбор анамнеза, общий осмотр пациентки с оценкой эндокринной, нервной, сердечно-сосудистой, дыхательной, пищеварительной, мочевыделительной и половой систем.
При гинекологическом исследовании оценку степени пролапса проводили в покое и при натуживании с определением ведущей точки пролапса по классификации POP-Q. Выявление и определение степени выраженности ДСТ у каждой пациентки проводили по балльной шкале поАббакумовой Л.Н.[18]. При первой степени тяжести ДСТ (вариант нормы) сумма баллов не превышает 12 баллов, при умеренной — 23, при выраженной степени тяжести — 24 и более.
Ультразвуковое исследование (УЗИ) органов малого таза и мочевыделительной системы выполняли с помощью ультразвуковых аппаратов General Electric Logic-400 (США), Sonoline G 60 S (ФРГ) и Aloka SSD 1400 (Япония). Производили абдоминальное, влагалищное и промежностное сканирование с использованием датчиков 3,5; 5,0 и 7 МГц.
При УЗИ оценивали форму, размеры и положение мочевого пузыря и матки, их патологические изменения, состояние придатков, объем остаточной мочи, конфигурацию шейки мочевого пузыря, состояние уретры и периуретральных тканей, задний уретровезикальный угол, подвижность уретровезикального сегмента, состояние мышечных и связочных структур тазового дна, наружный и внутренний сфинктеры заднего прохода, высоту и степень выраженности сухожильного центра промежности, состояние ректовагинальной перегородки, деформацию контура передней стенки прямой кишки [13].
Отдаленные результаты оперативного вмешательства были прослежены у больных в сроки от 1 до 5 лет. Контрольное обследование пациенток проводили в сроки 1, 3, 6 и 12 месяцев после операции, затем ежегодно. Статистическую обработку массива данных проводили на персональном компьютере с помощью электронных таблиц «Microsoft Excel» и пакета прикладных программ «Statistica for Windows» v. 7.0, StatSoft Inc. (США).
Рассчитывали следующие показатели: среднее арифметическое (М); стандартное отклонение (СО); коэффициент вариации; асимметрию и эксцесс с оценкой их репрезентативности по t-критерию Стьюдента; коэффициент корреляции (r); степень вероятности возможной ошибки (p). При оценке существенности различий между средними величинами вычисляли коэффициент достоверности по критериям Стьюдента. За уровень достоверности была принята вероятность различия 95,0% (p≤0,05).
Для выявления доли факториального и случайного влияния проводили дисперсионный анализ полученных результатов. Коэффициент корреляции и его достоверность рассчитывали по Браве-Пирсон, где 0,3–0,5 – умеренная, 0,5–0,7 – значительная и 0,7–0,9 – сильно выраженная связь.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В ходе исследования установлено, что средний возраст пациенток варьировал от 46 лет до 81 года и составил в I группе соответственно 58±11,7, во II – 59,5±8,7 (p>0,05). Средняя продолжительность заболевания в группах составила соответственно 7,7±5,5 и 7,5±6,0 (p>0,05), а возраст появления первых симптомов ПГ – 50,6±6,5 и 51,1±5,4 года, соответственно (p>0,05). Распределение пациенток по стадиям ПГ POP-Q представлено в таблице 2 и было сопоставимо между собой. IV стадия ПГ выявлена у 24,3% пациенток, III стадия – у 51,5%.
Таблица 2. Распределение пациенток по классификации POP-Q,%
|
Группы |
Стадия пролапса |
|||||||||
|---|---|---|---|---|---|---|---|---|---|---|
|
Ba II |
Ba III |
Ba IV |
Bp 1 |
Вр II |
Bp III |
BpIV |
CHI |
CIV |
Элонгация шейки матки |
|
|
I |
23,3 |
55.8 |
20,9 |
4,7 |
4,7 |
7,0 |
2,3 |
14.0 |
14,0 |
25,6 |
|
II |
26,0 |
54,0 |
20.0 |
6,0 |
6,0 |
6,0 |
2,0 |
14,0 |
14,0 |
24,0 |
|
Всего |
24,7 |
54,9 |
20,5 |
5,4 |
5,4 |
6,5 |
2,2 |
14,0 |
14,0 |
24,8 |
Примечание — различия недостоверны при сравнении групп (р>0,05)
Частота заболеваний, сопровождающихся повышением внутрибрюшного давления (ХОБЛ, запоры), составила в I группе 30,2% и во II — 30,0%. В постменопаузе находилось 90,7% пациенток I группы и 90,0% — II (p>0,05). Почти у каждой пятой пациентки в обеих группах причиной менопаузы была ранее перенесенная гистерэктомия. Умеренная и выраженная степень тяжести ДСТ по результатам оценки фенотипических признаков ДСТ по Аббакумовой Л.Н. выявлена у 66,0% пациенток.
Результаты нашего исследования коррелируют с исследованием Чечневой М.А., так анализ данных эхографии тазового дна выявил у 66,9% пациенток характерные для ПГ изменения (табл. 3)[13]. Истончение мышечных пучков ножек леваторов (m. bulbocavernosus) в среднем до 1±0,4 см, диастаз мышц в области сухожильного центра в среднем до 1,9±1,3 см, деформацию и уменьшение высоты сухожильного центра в среднем до 0,9±0,4 см. Дефекты тазовой фасции диагностированы у всех пациенток.
Таблица 3. Показатели структур тазового дна у пациенток до операции по данным УЗИ, см (М±СО)
|
Группы |
Высота сухожильного центра |
Ширина m. bulbocavernosus |
Диастаз m. levator |
|---|---|---|---|
|
I |
0,9±0,4* |
1±0,4* |
2,0±1,3* |
|
II |
0,9±0,4* |
1±0,4* |
1,8±1,3* |
|
Норма |
1,0-2,4 |
1,4-2,2 см |
Нет диастаза |
|
Примечание — *различия достоверны при сравнении показателей с нормативными (р<0,05) |
|||
У всех женщин с ректоцеле (25,5% и 22,0% пациенток в I и IIгруппах соответственно) при УЗИ выявлена деформация контура прямой кишки в виде «мешковидного» выпячивания стенки. Достоверных различий между исследованными группами по результатам УЗИ не выявлено (p>0,05). Средняя длительность оперативного вмешательства зависела от объема операции и составила 50,9±20,9 и 55,7±19,7 мин в I и II группах соответственно (p>0,05).
Рассматривая структуру рецидивов ПГ (табл. 4), необходимо отметить, что анатомическим (объективным) рецидивом ПГ мы считали появление пролапса II и последующих стадий по классификации POPQ (ICS, 1996). Согласно данным мировой литературы при оперативном лечении ПГ собственными тканями рецидивы возникают до 40% [14,19,20]. Эффективность использования сетчатых имплантатов по данным литературы достигает 80,5% – 95,8% [1,7,10,14,21].
Таблица 4. Рецидивы ПГ, n (%)
|
Группа |
Изолированное цистоцеле 11-111 ст |
Изолированное |
Сочетание цистоцеле II-III ст. с ректоцеле II-III ст. |
апикальный пролапс II-III ст. |
цисторектоцеле II-III ст. с апикальным пролапсом II-III ст. |
Всего |
|---|---|---|---|---|---|---|
|
I |
20,9* |
2,3* |
25,6* |
2,3 |
4,7* |
55,8* |
|
II |
0 |
10,0 |
0 |
0 |
0 |
10,0 |
Примечание — *различия достоверны при сравнении показателей 1 группы с II и III группами (р<0,05)
Наши данные коррелируют с исследованиями других авторов. В послеоперационном периоде, через 6 месяцев после операции, рецидив ПГ выявлен у 55,8% пациенток I группы и у 10,0% — II (p<0,05). Большинство рецидивов ПГ (53,5%) диагностированы у пациенток I группы в оперированных отделах в отличие от пациенток, оперированных с помощью сеток (0% во II, p<0,05), что свидетельствует о меньшей эффективности операций собственными тканями.
По данным УЗИ тазового дна пациенток двух групп через 6 месяцев после операции отмечено статистически значимое увеличение высоты сухожильного центра и уменьшение диастаза леваторов в сравнении с дооперационными значениями, при этом ширина m. bulbocavernosus осталась неизменной (рис. 1,2). Сравнение числа пациенток с ультразвуковыми признаками дефекта лобково-шеечной фасции до и после операции выявило их достоверное уменьшение в 2 группах (рис. 3).
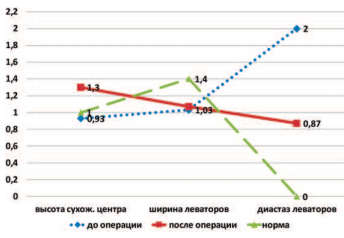
Рис. 1. Динамика изменения размеров структур тазового дна до и после операции у пациенток I группы
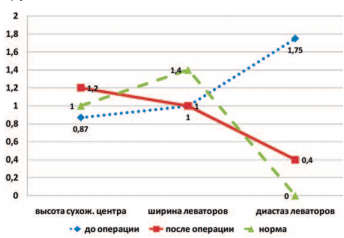
Рис. 2. Динамика изменения размеров структур тазового дна до и после операции у пациенток II группы
Межгрупповой анализ числа пациенток с эхографическими признаками дефекта лобково-шеечной фасции после операции доказал большую (в 17 раз) эффективность вагинальной экстраперитонеальной кольпопексии полипропиленовым имплантом в сравнении с пластикой передней стенки влагалища собственными тканями (7,0% против 51,2%). Число пациенток с признаками дефекта ректо-вагинальной фасции оказалось в 3 раза больше в I группе (32,6%) в сравнении со II (10,0%), что свидетельствует о меньшей эффективности вагинальных операций по коррекции ректоцеле собственными тканями, чем с использованием полипропиленовых сеток (рис. 3).
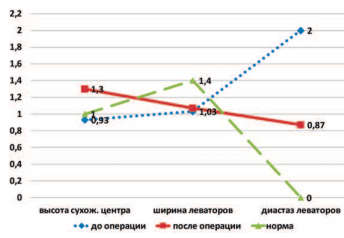
Рис. 3. Динамика количества пациенток I и II групп с ультразвуковыми признаками дефекта лобковошеечной и ректо-вагинальной фасций до и после операции
Проведенный корреляционный анализ в I группе выявил наличие сильной связи рецидива ПГ со степенью выраженности ДСТ (r=0,78; p<0,01) и длительностью заболевания (r=0,73; p<0,01). Статистически значимой связи рецидива ПГ с заболеваниями, сопровождающимися повышением внутрибрюшного давления, и с фактом гистерэктомии в анамнезе, не выявлено. Длительность болезни у пациенток I группы с рецидивом ПГ после оперативного лечения и без рецидива ПГ достоверно отличалась (p<0,01) и составила 11,3±4,6 и 3,3±2,5 года, соответственно.
Среди пациенток I группы с рецидивом ПГ после оперативного лечения у 54,0% выявлена умеренная и у 45,8% — выраженная степень ДСТ, что достоверно отличается от пациенток без рецидива ПГ, среди которых у 73,7% и у 26,3% была легкая и умеренная степень ДСТ. УЗИ промежности до операции у пациенток I группы выявило достоверно худшие показатели размеров структур тазового дна у женщин с рецидивом ПГ в сравнении с аналогичными показателями у пациенток без рецидива (рис. 4).
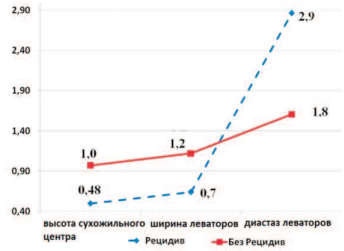
Рис. 4. Размеры структур тазового дна до операции у пациенток I группы с рецидивом ПГ и без рецидива (по данным УЗИ)
Корреляционный анализ установил наличие связи между показателями структур тазового дна по данным УЗИ со степенью выраженности ДСТ. Так, высота сухожильного центра и ширина m. bulbocavernosus имели сильную степень корреляции (r=-0,8; p<0,01 и r=-0,86; p<0,01, соответственно), диастаз леваторов — значительную (r=0,55; p<0,01). Значительная корреляция также выявлена между шириной m. bulbocavernosus по данным УЗИ и длительностью заболевания (r= -0,66; p<0,01).
Таким образом, установлена низкая эффективность оперативной коррекции ПГ собственными тканями и высокий риск его рецидива у пациенток с выраженной и умеренной ДСТ, длительностью болезни более 10 лет и имеющих выраженные ультразвуковые признаки несостоятельности мышц тазового дна. У пациенток II группы корреляционный анализ выявил умеренную связь рецидива ПГ в неоперированном отделе со степенью выраженности ДСТ (r=0,47; p<0,01).У всех пациенток с рецидивом ректоцеле после оперативного лечения выявлена более выраженная степень тяжести ДСТ в отличие от пациенток без рецидива ПГ, у которых выраженная ДСТ выявлена только у 1,6%.
Сравнительный анализ размеров структур тазового дна по данным УЗИ выявил, что у пациенток с рецидивом ректоцеле и у женщин, имевших ректоцеле до операции, ультразвуковые показатели структур тазового дна до операции статистически достоверно (p≤0,05) хуже, чем аналогичные показатели у пациенток без рецидива ПГ. Достоверных различий ультразвуковых показателей структур тазового дна до операции у пациенток с рецидивом ПГ и с коррекцией ректоцеле полипропиленовой сеткой и без рецидива выявлено не было (p>0,05).
Длительность болезни у пациенток II группы, условно разделенных по принципу наличия рецидива ректоцеле, достоверно не отличалась между собой и составила 6,4±2,5 года у пациенток с рецидивом ректоцеле и 5,7±4 года — без рецидива пролапса и без ректоцеле до операции (p>0,05). Выявлена корреляционная связь между показателями структур тазового дна по данным УЗИ и степенью выраженностиДСТ. Так, высота сухожильного центра и ширина m. bulbocavernosus имели выраженную корреляцию со степенью ДСТ (r=-0,76; p<0,01 и r=- 0,77; p<0,01 соответственно), диастаз леваторов – значительную (r=0,59; p<0,01), а диастаз леваторов и длительность заболевания – умеренную (r=0,43; p<0,01).
Наши данные коррелируют с исследованиями многих авторов доказывающих роль ДСТ в патогенезе ПГ, а также рецидива данного заболевания [22,23]. Таким образом, улучшение ультразвуковых показателей структур тазового дна и устранение дефектов лобково-шеечной и ректовагинальной фасций у пациенток II группы свидетельствуют о высокой эффективности вагинальной экстраперитонеальной кольпопексии полипропиленовымимплантом. Более того, мы считаем, что выявленная корреляция между повреждениями структур тазового дна по УЗИ и степенью выраженности ДСТ у пациенток II группы, значимо повлияла на возникновение рецидива ректоцеле (r=0,47; p<0,01).
ЗАКЛЮЧЕНИЕ
Коррекцию пролапса гениталий влагалищным доступом с использованием полипропиленовых имплантов целесообразно проводить пациенткам с рецидивными формами заболевания, с выраженной и умеренно выраженной степенью ДСТ, длительностью болезни более 10 лет и имеющих выраженные ультразвуковые признаки несостоятельности мышц тазового дна: высоту сухожильного центра менее 0,7±0,3 см, ширину m. bulbocavernosus менее 0,7±0,2 см и диастаз леваторов более 2,8±0,5 см
ЛИТЕРАТУРА
- Nygaard I, Brubaker L, Zyczynski HM, Cundiff G, Richter H, Gantz M, et al. Long-term outcomesfollowing abdominal sacrocolpopexy for pelvic organ prolapse. JAMA 2013;309:(19): 2016–2024. doi: 10.1001/jama.2013.4919.
- Шарифулин М.А., Протопопова Н.В., Кравченко Н.А., Бурдукова Н.В. Коррекция пролапса гениталий с помощью синтетических материалов. Сибирский медицинский журнал 2012;(7):121–122.
- Малхасян, В.А.Анатомо -функциональное состояние нижнихмочевых путей у женщин с пролапсом тазовых органов после экстраперитонеальной вагинопексии (операция Prolift) : автореф. дис. … канд. мед. наук М. 2012. 25 с.
- Абрамян,К.Н. Профилактика и лечение осложнений экстраперитонеальной вагинопексии (операции Prolift): автореф. дисс. ... канд. мед. наук. М.; 2011. 25 с.
- Салимова,Л.Я.К.Хирургическое лечение пролапса гениталий влагалищнымдоступом: автореф. дисс. … д-ра мед. наук. М.; 2012. 33 с.
- Шкарупа Д.Д., Шпиленя Е.С., Кубин Н.Д. Основные проблемы, ассоциированные с применением синтетических сетчатых эндопротезов во влагалищной хирургии недержания мочи и тазового пролапса на современном этапе. Медицинский вестник Башкортостана 2013;8(3):172-175.
- ШкарупаД.Д.,КубинН.Д.Протезирующая реконструкция тазового дна влагалищнымдоступом: современный взгляд на проблему. Экспериментальная и клиническая урология 2015;(1):88-93.
- Altman D, Väyrynen T, Engh ME, Axelsen S, Falconer C; Nordic Transvaginal Mesh Group. Anterior colporrhaphy versustransvaginal mesh for pelvic-organ prolapsed. N Engl J Med 2011;364(19):1826-36. doi: 10.1056/NEJMoa1009521.
- Withagen MI, MilaniAL, den Boon J, Vervest HA, Vierhout ME. Trocar-guided mesh comparedwith conventional vaginal repair in recurrent prolapse: a randomized controlled trial. Obstet Gynecol 2011;117(2Pt1):242-50. doi: 10.1097/AOG.0b013e318203e6a5.
- Филимонов В.Б., Васин Р.В., Васина И.В., КапринА.Д., КостинА.А. Оперативное лечение генитального пролапса с применением сверхлегких полипропиленовых сеток. Урология 2017;(2):14-23.
- Шкарупа Д.Д. Хирургическая реконструкция тазового дна у женщин при недержании мочи и пролапсе тазовых органов (клинико-экспериментальное исследование): автореф. дисс. … докт. мед. наук. СПб.; 2014. 44 с.
- Марченко, Т.Б. Ближайшие и отдаленные результаты хирургического лечения пролапса гениталий у женщин пожилого и старческого возраста: автореф. дисс. … канд. мед. наук. М.; 2015. 24 с.
- Чечнева М.А. Рациональная концепция комплексного обследования женщин с синдромомтазовой десценции и мочевой инконтиненцией: автореф. дисс. … докт. мед. наук. М.; 2011. 49 с.
- Maher C, Feiner B, Baessler K, Schmid C. Surgical management of pelvic organ prolapse in women. Cochrane Database Syst Rev 2013;(4):CD004014. doi: 10.1002/14651858.CD004014.pub5.
- Филимонов В.Б., Васин Р.В., Каприн А.Д., Костин А.А., Васина И.В. Способ вагинальной экстраперитонеальной кольпопексии перфорированным имплантатом. Патент РФ № 2538796 МПК А61 В17/42. (2006.01); заявка № 2013102790/14, 05.02.2013, опуб.10.01.2015. Бюл.1.
- Перинеология: Болезни женской промежности в акушерско-гинекологических, сексологических, урологических, проктологических аспектах [Под ред. В.Е. Радзинского]. М.: ООО «Медицинское информационное агентство», 2006. 336 с.
- McCall ML. Posterior culdeplasty; surgical correction of enterocele during vaginal hysterectomy; a preliminary report. Obstet Gynecol 1957;10(6):595-602.
- Аббакумова Л.Н. Клиническиеформыдисплазии соединительной ткани у детей.Учебное пособие. СПб., 2006. 36 с.
- Zyczynski HM, Carey MP, Smith AR, Gauld JM, Robinson D, Sikirica V,et al. One-year clinical outcomes after prolapse surgery with nonanchored mesh and vaginal support device. Am J Obstet Gynecol
2010;203(6):587.e1-8. doi: 10.1016/j.ajog.2010.08.001. - Miller D, Lucente V, Babin E, Beach P, Jones P, Robinson D. Prospective clinical as-sessment of the transvaginal mesh technique fortreatment of pelvic organ prolapse 5-yearresults. Female Pelvic Med Reconstr Surg 2011;17(3):139-43. doi: 10.1097/SPV.0b013e3182175da6.
- Тарасов Н.И., Шульгин А.С. Коррекция функции мочевых путей при пролапсе тазовых органов у женщин. Медицинский вестник Башкортостана 2013;8(2):152-156.
- Камоева С.В., Савченко Т.Н., ИвановаА.В.,Абаева Х.А. Современные генетические аспекты пролапса тазовых органов у женщин. Акушерство гинекология репродукция 2013;7(1):17
- ХитарьянА.Г.,ДульеровК.А. , ПогосянА.А., Полонская Е.И., Проворотов М.Е.Анатомо-функциональное состояние мышц тазового дна и ректовагинальной перегородки у женщин с задним тазовым пролапсом и ректоцеле. Практическая медицина 2013;67(2): 90-94.



