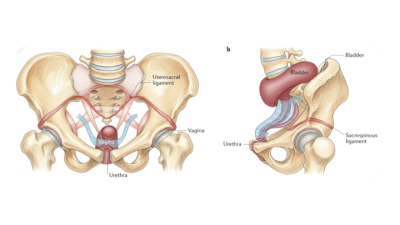
РАК – НЕ ПРЕПЯТСТВИЕ РОЖАТЬ
Статистика ВОЗ показывает, что на сегодняшний день в мире около 25 миллионов человек страдают онкологическими заболеваниями. Ежегодно диагностируется более 12 миллионов новых случаев рака, около семи миллионов пациентов с этим диагнозом умирают. К сожалению, 15% раковых заболеваний выявляются у пациентов не старше 55 лет, а трети из них нет даже 20-ти. Эксперты ВОЗ к 2020 году прогнозируют двукратное увеличение онкобольных.
Однако, современная медицина позволяет женщинам с онкологией разной сложности и локализации выживать, и показатель выживаемости у большинства из них в возрасте 15-54 лет достигает 75%.
Специалисты НИИ акушерства и гинекологии (ГБУЗ МО МОНИИАГ, Москва) К. В. Краснопольская, Т. А. Назаренко и О. С. Балахонцева исследовали подходы в сохранении репродуктивной функции у женщин с онкологическими заболеваниями в России и за рубежом.
Неоспоримо, что увеличение женщин репродуктивного возраста с онкологическими заболеваниями делает актуальным развитие технологий, обеспечивающих девушкам (женщинам) способность рожать. По мнению авторов, методы, позволяющие онкологическим пациенткам испытать радость материнства, условно можно разделить на три группы. Это – органосохраняющие операции при опухолях половых органов, методические приёмы ослабления гонадотоксического эффекта радио- и химиотерапии и вспомогательные репродуктивные технологии и методы криоконсервации генетического материала.
Резать не значит вырезать
Лечение неоплазий шейки и тела матки, а также яичников подавляющем большинстве требует удаления поражённых органов. После такой операции женщина, как правило, не может беременеть, и поэтому в лечении опухолей половой системы актуальны разработки по внедрению в практику щадящих органосохраняющих операций. Это значит, что хирургическое вмешательство должно быть не только эффективным, но и дарить женщине возможность иметь детей.
На начальной стадии рака шейки матки (карцинома in situ) ампутация шейки матки оправдана, но даже после такой операции наступление беременности нельзя исключать.
Полная ампутация целесообразна в том случае, если пациентка не заинтересована иметь детей, или перспективы успешного деторождения крайне малы. При лечении РШМ в настоящее время разработаны такие варианты функционально-щадящего лечения, как транспозиция яичников.
Высокие показатели выживаемости женщин с микроскопической онкологией (93-95%), перенёсших только хирургическое лечение, создали предпосылку для разработки расширенных операций по удалению шейки матки, но с сохранением возможности деторождения.
Пограничные опухоли яичников низкой степени злокачественности у женщин молодого и среднего возраста встречаются чаще, чем карциномы. Поэтому специалисты рекомендуют органосохраняющее лечение с последующим динамичным наблюдением у онколога. В ряде случаев при инвазивном раке яичников допускается удаление только одного яичника. И сохранение второго яичника допустимо только у молодых пациенток.
Однако специалисты признают, что диагностика неоплазий яичников на ранних стадиях затруднительна из-за отсутствия четких симптомов и признаков. Поэтому клиницисты сталкиваются с такими пациентками, когда у них заболевание на поздней стадии, при котором органосохраняющее лечение невозможно.
В настоящее времени уже доказаны положительные результаты гормонотерапии как самостоятельного метода лечения молодых пациенток с атипической гиперплазией и начальными формами высокодифференцированной аденокарциномы эндометрия. При лейомиосаркомах матки метастатическое поражение яичников крайне мало, и это позволяет сохранять придатки.
Некоторые исследования показали, что у молодым пациенткам с опухолями внутренних половых органов можно сохранять детородную функцию на ранних стадиях рака матки и яичников за счет выполнения альтернативных операций, а также при аденокарциноме без разрастания опухоли. При односторонних опухолях парных органов, можно сохранять непоражённый яичник. И, конечно же, всем пациенткам необходимо регулярно обследоваться у онколога.
Эффекты противоопухолевой терапии
Эффективность современной онкологии обеспечивают широкое применение химиотерапии и радиотерапии. Однако, несмотря на то, что эти методы лечения сохраняют пациенткам жизнь, зачастую они сводят на нет возможность иметь детей из-за высокотоксичного действия на яичники.
Конечно же подавляющее большинство женщин хотят и надеются, что смогут рожать, несмотря на комплексное противоопухолевое лечение. Поэтому наука разрабатывает методы онкотерапии, с низким негативным воздействием ионизирующей радиации и цитостатических препаратов. На сегодня набор таких методов ограничен – по сути, метод один – транспозиция яичников перед облучением малого таза и подавление функции яичников во время химиотерапии.
Транспозиция яичников только ослабляет радиотоксический эффект, и все-таки ускоряет наступление менопаузы. Преждевременному старению яичников способствует не только облучение, но и нарушение кровообращения, в том числе из-за операционных манипуляций, считай - ошибок.
Подавление функции яичников, по мнению специалистов, в период химиотерапии может позитивно влиять на фолликулярный аппарат и снижать риск преждевременной менопаузы.
Авторы исследования отмечают, что фармакологическая блокада яичников не защищает их от последствий облучения. Кроме того, не все специалисты считают, что подобные препараты являются защитниками женских придатков в период химиотерапии. Так, экспертная группа на XI Международной конференции по терапии ранних форм рака молочной железы в Сан-Галлене (Швейцария, 2009г) рекомендовала пересмотреть положение о целесообразности методов сохранения фертильности путём противодействия гонадотоксичному эффекту цитостатиков с помощью препаратоов, вызывающих десенситизацию аденогипофиза.
Роды после замораживания – реальность
Репродуктологи считают, что возможность рожать женщинам с онкологическими заболеваниями позволит криоконсервация эмбрионов, зрелых и незрелых яйцеклеток, а также яичниковой ткани.
Получение этих материалов необходимо производить до начала химио- и лучевой терапии, и использовать для стимуляции беременности на любых сроках (без ограничений!) после завершения противоопухолевой терапии. Каждый из методов криоконсервации имеет свои преимущества и недостатки, поэтому подбирать оптимальное лечение необходимо индивидуально.
Криоконсервация эмбрионов с последующим размораживанием и перенос пациентке в естественном цикле, широко применяются во всех центрах ВРТ. Эта процедура эффективна по частоте наступления беременности в каждом четвёртом случае (26%). Именно криоконсервация эмбрионов широко используется для сохранения фертильности онкобольных. Эта методика хорошо отработана, так как используется более длительное время, чем криоконсервация ооцитов и яичниковой ткани.
Криоконсервация зрелых яйцеклеток вместо замораживания эмбрионов практикуется в центрах ВРТ в тех случаях, когда у пациентки нет партнёра и, соответственно, нет возможности оплодотворить зрелые яйцеклетки. Некоторые женщины настаивают на консервации яйцеклеток, а не эмбрионов, чтобы в будущем избежать в будущем юридических и моральных проблем.
Современная криоконсервация зрелых яйцеклеток позволяет обеспечить их выживаемость на уровне 90%, при том, что их способность к оплодотворению сопоставима и даже не отличается от свежеполученных яйцеклеток – таковы данные получили японских специалистов. Их европейские коллеги менее оптимистичны. Но все сходятся во мнении, что вопрос криоконсервации яйцеклеток требует детального изучения.
Открытой остаётся дискуссия: каким должен быть идеальный протокол стимуляции яичников?
Авторы публикации обращают внимание на то, что для предотвращения типичного для суперовуляции предовуляторного подъема эстрадиола можно вообще отказаться от назначения индукторов овуляции и получать яйцеклетки в нестимулируемом цикле. Однако, получение единственного ооцита и, в случае его успешного оплодотворения, – единственного эмбриона не дают гарантии сохранения этого эмбриона из-за криотравм при его замораживании и оттаивании. Да и перенос единственного эмбриона всегда снижает вероятность успешной имплантации. По этой причине на практике специалисты осуществляют перенос нескольких эмбрионов, отбираемых, как лучшие из имеющихся. Очевидно, что получение большого количества эмбрионов с целью их отбора для последующего переноса возможно лишь при использовании в программе ЭКО индукторов овуляции, обеспечивающих мультифолликулярный ответ. Все это не позволяет широко использовать программу ЭКО в естественных циклах у онкологических больных.
И отечественные и зарубежные специалисты считают, что проблема выбора идеального протокола для стимуляции яичников у онкологических больных пока не решена из-за отсутствия масштабных исследований.
Как оказалось, идеального протокола среди схем использования гонадотропинов вообще не существует. При использовании «мягкой» стимуляции увеличивается риск бедного ответа, минимизирующего число получаемых и сохраняемых эмбрионов. И для онкобольных – это драматический вариант, из-за невозможности повтора.
При отдельном рассмотрении вопроса о допустимости стимуляции яичников у онкобольных, авторы исследования, ссылаясь на приказ Минздрава РФ №67, напоминают, что наличие онкологической патологии в истории болезни является противопоказанием к ЭКО. А это значит, что использование индукторов овуляции женщинам с онкологией запрещено. Авторы отмечают, что такое ограничение характерно лишь для российской медицины. Зарубежные специалисты в разных странах сообщают о стимуляции яичников в рамках программ получения и сохранения эмбрионов или зрелых яйцеклеток у женщин с различными видами неоплазий.
Авторы считают, что для активации в России исследований по сохранению фертильности у онкологических пациенток методом криоконсервации генетического материала давно пора отказаться от ряда явно устаревших положений и разрешить использование индукторов овуляции у пациенток со злокачественными опухолями.
Подавляющее большинство зарубежных специалистов считает, что временные гормональные сдвиги, возникающие из-за приема стимуляторов овуляции, а также двухнедельная задержка начала химиотерапии или радиотерапии не влияют на результаты противоопухолевой терапии
Авторы не сомневаются, что в действительности на результат лечения злокачественных новообразований влияют особенности самой опухоли и выбранная противоопухолевая терапия, а также состояние иммунитета, а не временные изменения в гомеостазе, вызванные индукторами овуляции при получении генетического материала для сохранения фертильности
Суть метода криоконсервации незрелых яйцеклеток в том, что пациентке в нестимулированном цикле на восьмой день вводят спецпрепарат и через 36 часов выделяют все видимые фолликулы. Все незрелые яйцеклетки культивируют в специальных средах в течение суток-двое до подтверждения их зрелости по методике IVM (in vitro maturation). Затем яйцеклетки замораживают и в таком виде сохраняют сколь угодно долго. В случае необходимости яйцеклетки размораживают, проводят инсеминацию, и полученные эмбрионы через двое суток переносят в полость матки, если УЗИ подтверждает подготовленности эндометрия к процедуре имплантации.
Статистика показала, что беременность с использованием ооцитов, дозревших путём IVM, наступает в полтора-два раза реже, чем в программах со зрелыми ооцитами. Однако эту программу специалисты рекомендуют использовать, когда женщинам с онкологическими заболеваниями необходимо сократить время использования индукторов овуляции или вовсе от них отказаться. Это оправдано для женщин с повышенным риском синдрома гиперстимуляции яичников или с отклонением в гомеостазе.
Репродуктивный потенциал женщины можно увеличить и криоконсервацией кортикальной ткани яичника. После завершения противоопухолевой терапии предварительно полученную кортикальную ткан яичника размораживают и вновь вживляют на место. Для пересадки может быть выбран как сохранённый нефункционирующий яичник, так и перитонеальное пространство, и даже подкожные участки предплечья или передняя брюшная стенка.
Достоинством этого метода криоконсервации тканей яичника является легкость его выполнения.
Некоторые специалисты считают допустимым комбинирование лапараскопической операции забора яичниковой ткани со стимуляцией яичников, которую можно проводить уже через 1-3 суток после хирургического вмешательства на яичниках. Использование двух методов сохранения репродуктивной функции – криоконсервация ткани яичников и криоконсервация зрелых ооцитов или эмбрионов – существенно увеличивает шансы на преодоление бесплодия в будущем. После аутотрансплантации восстановление овулиции яичников наступает через четыре месяца после пересадки. Полноценное функционирование продолжается от двух – до пяти лет, и функциональная активность зависит от объема и качества пересаженной кортикальной ткани.
К сожалению, негативным фактором этого метода является возраст женщины. Абсолютным противопоказанием к обратной пересадке ткани яичника является наличие злокачественных клеток в выделенном материале.
Но в таком случае, специалисты рекомендуют выделение незрелых ооцитов из кортикальной ткани яичника и обеспечение их дозревания с помощью методики IVM. Полученные из пораженных раком яичников ооциты могут быть криоконсервированы и в последующем использоваться для зачатия. Этот метод применим не только у онкопациенток, но и у девочек.
Заключение
Успехи современной медицины обеспечивают не только выживание женщин с различными видами онкологических заболеваний, но и выполнение их главного предназначения – продолжения жизни.
Тем не менее, в области сохранения фертильности у онкобольных с помощью вспомогательных репродуктивных технологий в комбинации с криоконсервацией генетического материала, пока еще существует много нерешенных проблем как технических, так и организационных.
К техническим – научным – проблемам можно отнести отсутствие общепринятых стандартов и регламентирующих методик. Так, неясно, каким должен быть протокол стимуляции яичников у онкобольных пациенток, и может ли он быть в принципе.
К Техническим вопросам относятся хирургические приёмы аутотрансплантации яичниковой ткани, гарантирующие её приживление и последующее максимально продолжительное функционирование.
Организационная проблема – в отсутствии нормативных документов и стандартов, определяющих взаимодействие онкологов и репродуктологов при сохранении фертильности пациентки.
Кроме того, авторы призвали аннулировать Приказ № 67 МЗ РФ (2003г), как анахронизм, который запрещает использовать индукторы овуляции у онкологичеких больных.
Авторы отмечают, что очень (!) многим женщинам с онкологическими заболеваниями все ещё нет доступа к полной информации о современных методах сохранения фертильности. Ответственность за это несут специалисты-онкологи, которые наблюдают таких пациенток. По мнению авторов, эти специалисты также должны отвечать за поиск и поддержание рабочих контактов с центрами ВРТ, где пациентка будет беременеть и рожать.